Axit Là Gì? Cẩm Nang Toàn Tập Về Tính Chất, Phân Loại Và Ứng Dụng Thực Tế
Axit là một thuật ngữ vừa quen vừa lạ. Quen vì chúng ta gặp nó hàng ngày: vị chua trong quả chanh, giấm ăn trong bếp, hay chai nước tẩy rửa nhà tắm. Lạ vì khi nhắc đến axit, nhiều người chỉ nghĩ đến những hóa chất ăn mòn đáng sợ.
Vậy thực chất axit là gì? Tại sao chúng lại đóng vai trò quan trọng đến thế trong công nghiệp và sự sống? Làm thế nào để sử dụng chúng an toàn? Bài viết này sẽ giải mã toàn bộ kiến thức về axit, từ lý thuyết hóa học khô khan đến những ứng dụng thú vị mà bạn không ngờ tới.
Định nghĩa chính xác: Axit là gì?
Theo định nghĩa hóa học phổ biến nhất (thuyết Arrhenius), Axit là những hợp chất hóa học mà trong phân tử có chứa một hay nhiều nguyên tử Hydro liên kết với gốc axit.
Điều kiện tiên quyết để xác định một chất là axit: Khi tan trong nước, axit sẽ phân ly ra ion dương H+ (Cation Hydro). Chính ion H+ này là “thủ phạm” gây ra vị chua và tính chất ăn mòn đặc trưng của axit.
Công thức hóa học chung: HxA
(Trong đó: x là hóa trị của gốc axit, A là gốc axit)
Ví dụ điển hình bạn thường gặp:
- HCl (Acid Clohydric): Thành phần chính có trong dịch vị dạ dày giúp tiêu hóa thức ăn.
- H₂SO₄ (Acid Sulfuric): Được mệnh danh là “máu của công nghiệp hóa chất”.
- CH₃COOH (Acid Axetic): Chính là giấm ăn chúng ta dùng hàng ngày (ở nồng độ 2-5%).
Năm Tính chất hóa học và vật lý đặc trưng của Axit
Để nhận biết axit mà không cần máy móc phức tạp, bạn có thể dựa vào các tính chất sau. Đây cũng là những kiến thức nền tảng quan trọng trong chương trình Hóa học.
Tính chất vật lý dễ nhận biết
- Vị giác: Đa số các axit đều có vị chua. Ví dụ: Axit Citric trong chanh, Axit Malic trong táo, Axit Lactic trong sữa chua.
⚠️ Cảnh báo an toàn: Tuyệt đối KHÔNG ĐƯỢC NẾM thử các loại hóa chất trong phòng thí nghiệm hoặc hóa chất tẩy rửa, vì chúng có thể gây ngộ độc hoặc bỏng niêm mạc miệng ngay lập tức.
- Độ tan: Hầu hết axit tan rất tốt trong nước.
- Dẫn điện: Dung dịch axit có khả năng dẫn điện tốt (do chứa các ion chuyển động tự do).
Tính chất hóa học quan trọng
Làm đổi màu chất chỉ thị màu
Đây là cách nhanh nhất để kiểm tra độ pH của dung dịch:
- Giấy quỳ tím gặp axit sẽ chuyển sang màu Đỏ (với axit mạnh) hoặc màu hồng (với axit yếu).
- Dung dịch Phenolphthalein không đổi màu trong môi trường axit.
Tác dụng với kim loại (Ăn mòn kim loại)
Dung dịch axit phản ứng với các kim loại đứng trước Hydro trong dãy hoạt động hóa học (như Nhôm, Sắt, Kẽm, Magie…) để tạo thành muối và giải phóng khí Hydro bay lên.
Ví dụ: Khi nhỏ Acid Clohydric (HCl) vào đinh sắt (Fe), bạn sẽ thấy bọt khí sủi lên. Đó chính là khí Hydro.
c. Tác dụng với Bazơ (Phản ứng trung hòa)
Axit và Bazơ là hai thái cực đối lập. Khi gặp nhau, chúng triệt tiêu tính chất của nhau để tạo thành Muối và Nước. Phản ứng này rất quan trọng trong việc xử lý nước thải hoặc trung hòa axit dư trong dạ dày.
d. Tác dụng với Oxit Bazơ (Tẩy gỉ sét)
Bạn có biết tại sao người ta dùng axit để tẩy gỉ sắt không? Vì gỉ sắt chính là Oxit Bazơ. Khi gặp axit, lớp gỉ này sẽ bị hòa tan sạch sẽ.
Phân loại Axit: Không phải axit nào cũng nguy hiểm
Thế giới axit rất đa dạng, chúng thường được chia làm hai nhóm chính dựa trên nguồn gốc và hai nhóm dựa trên sức mạnh.
Phân loại theo nguồn gốc
| Loại Axit | Nguồn gốc | Đặc điểm | Ví dụ điển hình |
|---|---|---|---|
| Axit Vô cơ (Axit Khoáng) | Từ khoáng chất | Tính acid mạnh, khả năng ăn mòn cao, dùng trong công nghiệp | HCl, H₂SO₄, HNO₃ |
| Axit Hữu cơ | Thực vật, động vật, vi sinh vật (chứa nhóm Cacbon) | Tính acid yếu, an toàn hơn, dùng trong thực phẩm, mỹ phẩm | Acid Citric (chanh), Acid Axetic (giấm), Acid Formic (nọc kiến) |
Phân loại theo độ mạnh yếu (Khả năng phân ly)
- Axit mạnh: Khi tan trong nước, 100% phân tử phân ly thành ion. Dẫn điện cực tốt.Ví dụ: HCl, HNO₃, H₂SO₄
- Axit yếu: Chỉ một phần nhỏ phân tử phân ly.Ví dụ: H₂S, H₂CO₃ (trong nước ngọt có gas)
Thang đo pH và cách đo độ mạnh của Axit
Để biết chính xác một dung dịch có tính axit mạnh hay yếu, người ta dùng thang đo pH (Potential of Hydrogen). Thang đo này chạy từ 0 đến 14.
| Độ pH | Môi trường | Ví dụ thực tế |
|---|---|---|
| pH 0-1 | Axit cực mạnh | Axit trong ắc quy (Rất nguy hiểm) |
| pH 2 | Axit mạnh | Nước chanh, dịch vị dạ dày |
| pH 4-5 | Axit yếu | Cà phê, nước mưa sạch |
| pH 7 | Trung tính | Nước cất tinh khiết |
| pH > 7 | Bazơ (Kiềm) | Xà phòng, dung dịch tẩy rửa |
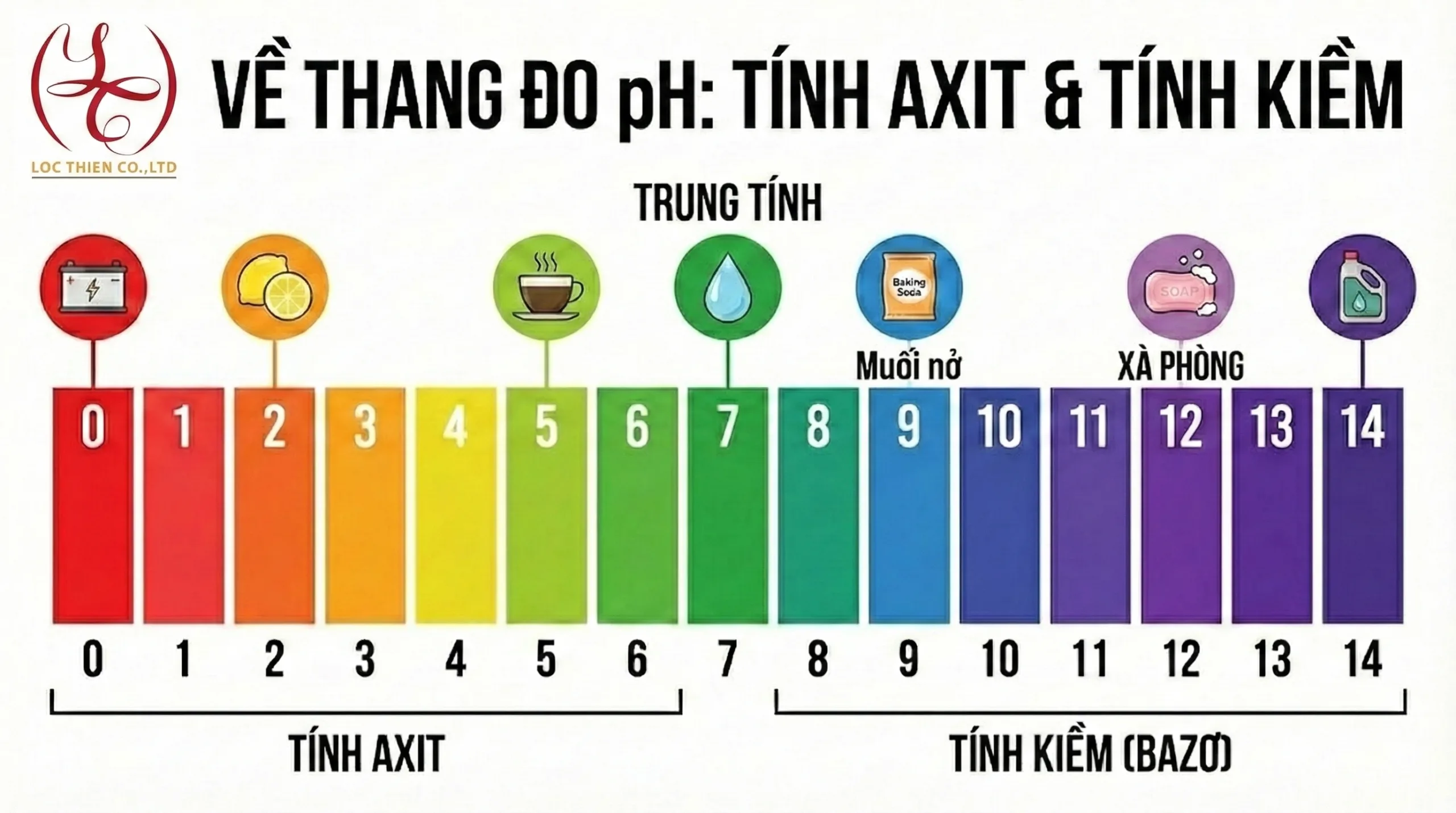
💡 Mẹo hay: Độ pH lý tưởng của da mặt người là 5.5 (hơi axit nhẹ) để bảo vệ da khỏi vi khuẩn. Nếu bạn dùng xà phòng có độ tẩy rửa quá mạnh (pH cao), lớp màng axit này sẽ bị phá hủy gây khô da.
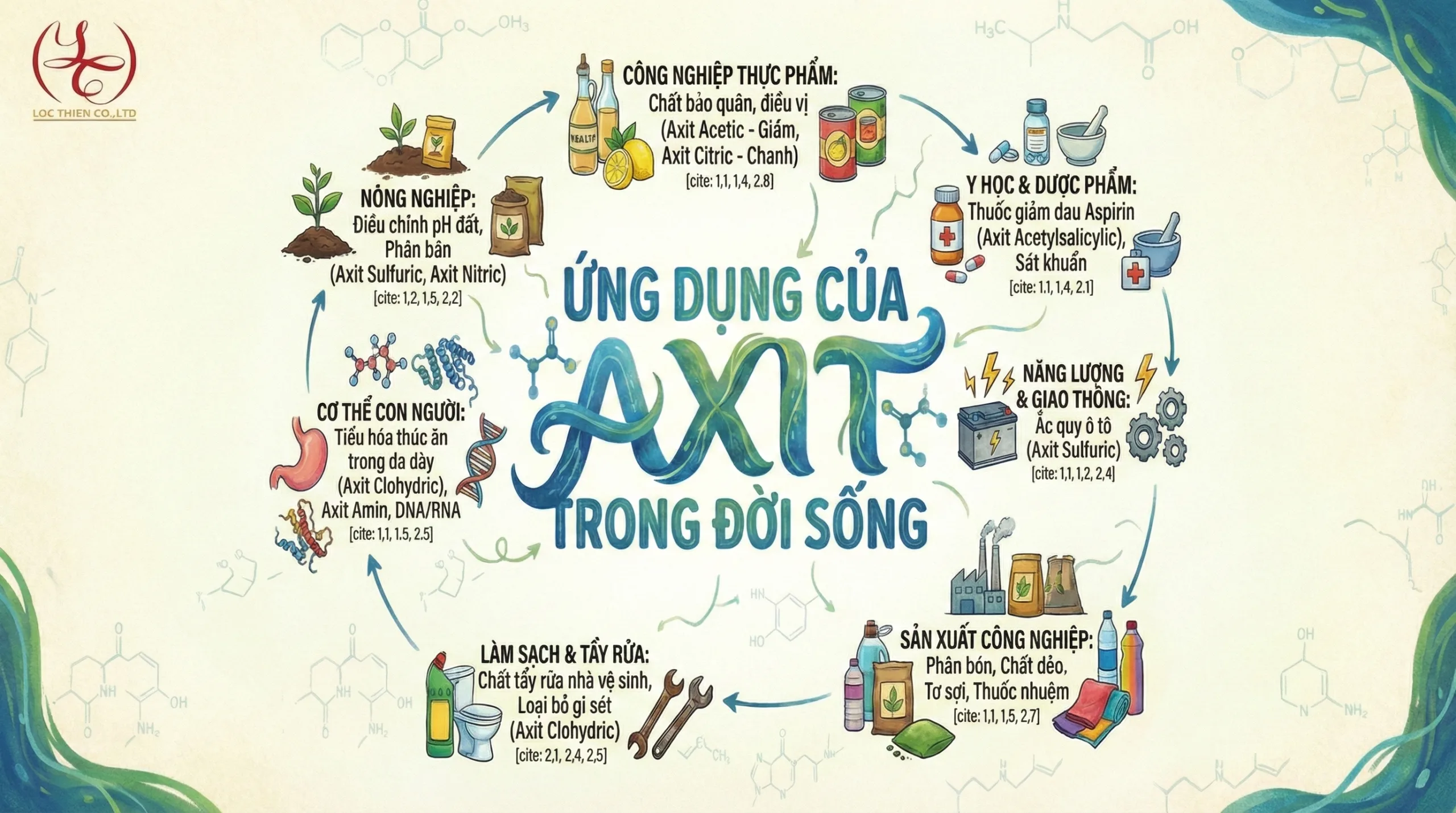
Ứng dụng thực tế của Axit trong đời sống
Nếu không có axit, nền văn minh công nghiệp hiện đại có thể sẽ sụp đổ. Dưới đây là những ứng dụng phổ biến nhất:
Trong công nghiệp nặng
- H₂SO₄ (Acid Sulfuric): Sản lượng tiêu thụ H₂SO₄ thường được dùng để đo lường sức mạnh kinh tế của một quốc gia. Nó dùng để sản xuất phân bón, lọc dầu, sản xuất sơn, chất dẻo.
- Ắc quy: Dung dịch điện ly trong bình ắc quy ô tô, xe máy chính là axit.
Trong Công nghiệp Thực phẩm (F&B)
- Chất tạo vị: Acid Citric, Acid Malic tạo vị chua thanh mát cho nước giải khát, bánh kẹo.
- Chất bảo quản: Acid Benzoic, Acid Sorbic giúp ức chế vi khuẩn, nấm mốc, kéo dài thời gian sử dụng thực phẩm đóng hộp.
Trong Y học và Làm đẹp (Skincare)
Đây là xu hướng đang rất “hot” trong cộng đồng làm đẹp:
- AHA (Alpha Hydroxy Acid) & BHA (Beta Hydroxy Acid): Dùng để tẩy tế bào chết hóa học, làm sáng da và trị mụn ẩn.
- Retinoic Acid: “Thần dược” chống lão hóa.
- Acid Folic: Vitamin quan trọng cho phụ nữ mang thai.
Trong Nông nghiệp
- Điều chỉnh độ chua của đất (cải tạo đất kiềm).
- Sản xuất thuốc trừ sâu và các loại phân bón Superphotphat.
Cẩm nang an toàn: Quy tắc vàng khi tiếp xúc với Axit
Axit, đặc biệt là axit đậm đặc, có thể gây bỏng sâu, hoại tử da và mù mắt nếu sơ ý. Bạn bắt buộc phải nhớ các quy tắc sau:
⚠️ Quy tắc “Sống Còn”: Cách pha loãng acid H₂SO₄
Khi muốn pha loãng axit sunfuric đậm đặc, bạn phải tuân thủ nguyên tắc:
“Rót TỪ TỪ Axit vào Nước, khuấy nhẹ”
TUYỆT ĐỐI KHÔNG LÀM NGƯỢC LẠI
Lý do: Acid H₂SO₄ cực kỳ háo nước và tỏa nhiệt mạnh. Nếu bạn rót nước vào axit, nước sẽ sôi đột ngột và bắn tung tóe axit ra ngoài gây bỏng nghiêm trọng.
🏥 Cách sơ cứu khi bị dính axit
- Rửa ngay lập tức: Xối rửa vùng da bị dính axit dưới vòi nước sạch mát chảy liên tục trong ít nhất 15-20 phút. (Không ngâm, hãy để nước chảy để cuốn trôi hóa chất).
- Cởi bỏ quần áo: Nhẹ nhàng loại bỏ quần áo dính hóa chất (trừ khi nó dính chặt vào da).
- Trung hòa (Chỉ khi có kiến thức): Có thể dùng dung dịch NaHCO₃ (Baking soda) loãng 2% để rửa lại.
- Đến cơ sở y tế: Che vết thương bằng gạc sạch (không bông gòn) và đến bệnh viện ngay.
Liên hệ với chúng tôi
Bạn cần tư vấn về hóa chất công nghiệp hoặc sản phẩm axit chất lượng cao?
Đội ngũ chuyên gia của Hóa Chất Lộc Thiên sẵn sàng hỗ trợ!
Hóa Chất Lộc Thiên là lựa chọn hoàn hảo, đảm bảo nguồn hàng ổn định, giá cả cạnh tranh, và dịch vụ chuyên nghiệp.
- 📞 Hotline: 0979 89 1929
- 📩 Email: locthien.info@gmail.com
- 🌐 Website: hoachatlocthien.com
- 🏠 Địa chỉ: 452/6B Tỉnh Lộ 10, P. Bình Trị Đông, Q. Bình Tân, TP.HCM
- 📱 Điện thoại: 028 6269 5669 – 028 6269 5662

Liên hệ ngay hôm nay để nhận báo giá tốt nhất và hỗ trợ giao hàng nhanh chóng!
Lộc Thiên không chỉ mang đến sản phẩm chất lượng mà còn đảm bảo sự an toàn và bền vững cho khách hàng và môi trường.
THANKYOU
Các câu hỏi thường gặp (FAQ) về Axit
A: Dùng giấy quỳ tím:
- Gặp Axit: Quỳ tím hóa ĐỎ.
- Gặp Bazơ: Quỳ tím hóa XANH.
Lời kết
Axit không chỉ là những chai hóa chất nằm im trong phòng thí nghiệm, chúng là một phần không thể thiếu của cuộc sống. Hiểu đúng về axit là gì, tính chất và cách sử dụng an toàn sẽ giúp bạn tận dụng được sức mạnh của chúng phục vụ cho công việc và đời sống, đồng thời tránh xa những rủi ro đáng tiếc.
Nếu bạn đang tìm kiếm các sản phẩm hóa chất công nghiệp hoặc cần tư vấn kỹ thuật chuyên sâu về xử lý axit, hãy để lại bình luận bên dưới để được giải đáp chi tiết nhé!




