Acid H2SO4 Là Gì? Tính Chất, Ứng Dụng Và Lưu Ý Sử Dụng
Acid H2SO4 (axit sulfuric) là một trong những hóa chất công nghiệp quan trọng nhất thế giới. H2SO4 là axit nhị chức, mạnh, có tính háo nước và oxy hóa, được dùng từ sản xuất phân bón đến acquy ô tô.
Noi dung tham khao, vui long doi chieu MSDS.

1. Acid H2SO4 là gì?
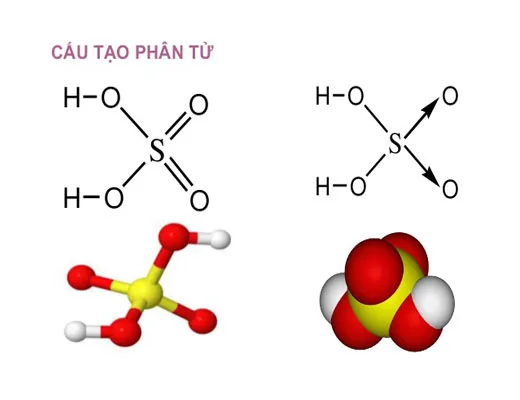
H2SO4 (axit sulfuric, vitriol) là axit vô cơ chứa 2 nguyên tử H, 1 nguyên tử S và 4 nguyên tử O. Trong tự nhiên, H2SO4 chỉ tồn tại trong các vùng núi lửa hoạt động. Trong công nghiệp, H2SO4 được sản xuất chủ yếu bằng quy trình Contact (đốt S → SO2 → SO3 → H2SO4).
2. Tính chất H2SO4
| Đặc điểm | Giá trị |
|---|---|
| Trạng thái | Lỏng nhớt, không màu hoặc vàng nhạt |
| Khối lượng riêng | ~ 1,84 g/mL ở 98% |
| Nhiệt độ sôi | 337°C ở 98% |
| Tính axit | Axit mạnh, nhị chức |
| Tính chất khác | Háo nước, oxy hóa, carbon hóa hữu cơ |
3. Ứng dụng của H2SO4
- Sản xuất phân bón (60% sản lượng toàn cầu).
- Sản xuất hóa chất cơ bản: HCl, HF, Na2SO4.
- Lọc dầu, hóa dầu.
- Luyện kim, thủy luyện.
- Acquy chì-axit.
- Xử lý nước thải.
4. Lưu ý quan trọng khi sử dụng H2SO4
- Pha loãng đúng: đổ axit vào nước, có khuấy.
- Bồn chứa thép cacbon (96–98%), thép không gỉ 316L hoặc PE/PP/PTFE tùy nồng độ.
- Cách ly với NaOH, kim loại kiềm, chất hữu cơ dễ cháy.
- PPE: kính, mặt nạ, găng tay butyl, ủng, tạp dề.
- Có vòi rửa khẩn cấp và phương án trung hòa Na2CO3, vôi.
Lien he Hoa Chat Loc Thien
Doi ngu ky thuat Hoa Chat Loc Thien san sang ho tro doanh nghiep.
- Hotline: 0979 89 1929
- Email: locthien@locthien.vn
- Website: hoachatlocthien.com/
FAQ
- Acid H2SO4 là gì?
H2SO4 là axit sulfuric – axit vô cơ mạnh nhị chức, có tính háo nước và oxy hóa. Đây là hóa chất công nghiệp có sản lượng lớn nhất thế giới. - Tại sao H2SO4 được gọi là ‘máu của ngành công nghiệp’?
Vì H2SO4 là nguyên liệu cơ bản cho hầu hết các ngành: phân bón, hóa chất, lọc dầu, luyện kim, acquy. Tiêu thụ H2SO4 thường được dùng làm chỉ báo phát triển công nghiệp của một quốc gia. - H2SO4 nồng độ nào phổ biến nhất?
Phổ biến nhất là H2SO4 98% (axit đặc), tiếp theo là 96% và 70%. Một số ngành đặc biệt dùng oleum 20% (H2SO4 + SO3) hoặc dung dịch loãng 30–37% (acquy). - Vì sao phải pha loãng H2SO4 cẩn thận?
Vì H2SO4 háo nước, phản ứng pha loãng tỏa nhiệt rất lớn (~880 J/g). Sai quy trình (đổ nước vào H2SO4) sẽ làm nước bốc hơi đột ngột, bắn axit nóng gây bỏng nặng. - Mua acid H2SO4 công nghiệp ở đâu?
Hóa Chất Lộc Thiên cung cấp H2SO4 70%/96%/98% với COA, MSDS, đóng can/IBC/xe bồn theo yêu cầu, kèm tư vấn kỹ thuật về kho chứa và xử lý sự cố.


